4. 水溶性大豆多糖類の詳細情報
製造方法
水溶性大豆多糖類は「オカラ」を原料に、弱酸性で抽出し、精製・殺菌・乾燥の工程を経て製造されます(図3)。水溶性大豆多糖類の成分分析値を表2に示します。水溶性大豆多糖類は、様々な糖が組み合わさってできた生体高分子物質であり、主要な構成糖はガラクトース、アラビノース、及び、ガラクツロン酸になります。カルボン酸を持ったガラクツロン酸を構成成分として含むことから、ペクチンと同じく、植物の細胞壁に含まれるペクチン性多糖類の一種と考えられています。
図3 水溶性大豆多糖類の製造工程
表2 水溶性大豆多糖類1)の成分分析値
| 水分 (%) |
粗タンパク質 (%) |
粗灰分 (%) |
食物繊維2) (%) |
構成糖組成3) (%) | ||||||
|---|---|---|---|---|---|---|---|---|---|---|
| Rha | Fuc | Ara | Xyl | Gal | Glc | GalA | ||||
5.8 |
9.2 |
8.6 |
66.2 |
5.0 |
3.2 |
22.6 |
3.7 |
46.1 |
1.2 |
18.2 |
1)ソヤファイブ-S-DNの代表分析値
2)AOAC法により分析した。
3)中性糖はアルジトールアセテート後GLCにより、ウロン酸はBlumenkrantz法で分析した。
大豆中のウロン酸はガラクツロン酸(GalA)である。
Rha: ラムノース, Fuc: フコース, Ara: アラビノース, Xyl: キシロース, Gal: ガラクトース, Glc: グルコース, GalA:ガラクツロン酸
多糖類としての基本的な性質
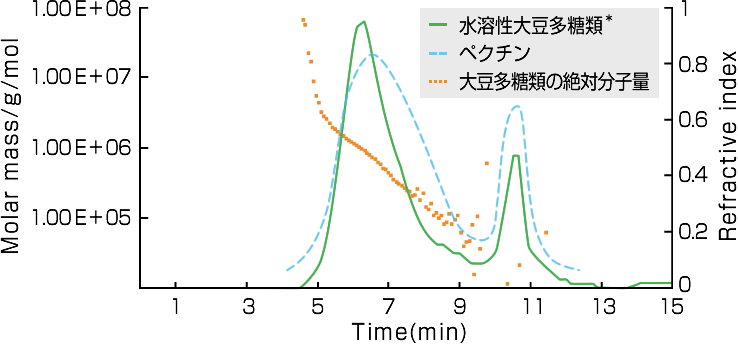
これまでお話してきました通り、水溶性大豆多糖類は糖質が複数結合して構成された多糖類です。その分子の大きさは、ゲル濾過クロマトグラフィーにより測定することが可能です。分析した結果を図4に示します。水溶性大豆多糖類は、分子サイズの異なる3成分(平均分子量550,000, 25,000, 5,000)から構成され、550,000の主成分が全体の70%を占めています。Prosky法で測定した粗繊維の含量は70〜80%と非常に高く、その水溶液は、グアーガムやペクチンのような増粘多糖類に比べて低い特性を示します(図5)。塩類を添加しても粘度の変化が少ないのも大きな特徴です。ペクチンは、カルシウムやマグネシウム等の二価のミネラルと反応して、増粘或いはゲルを形成します。
一方、水溶性大豆多糖類は、これら二価のミネラルと殆ど反応しないため、ペクチンのように増粘或いはゲル化剤として使用することが出来ません。その代わりに水溶性大豆多糖類は、この特徴を生かして、カルシウムや鉄などのミネラルを強化した食品を加工する際の安定剤として利用することが可能です。
図4 水溶性大豆多糖類の分子量分布
(HPLCの条件)
カラム: TSK-gel G-5000PWXL(東ソー)
溶離液: 0.1 M リン酸緩衝液, pH6.8
流量: 1.0 ml/min
検出器: RI & MALLS
(Wyatt Tech. DAWN EOS)
* ソヤファイブ-S-DA100を使用
図5 水溶性大豆多糖類の水溶液の濃度と粘度の関係 (25℃)
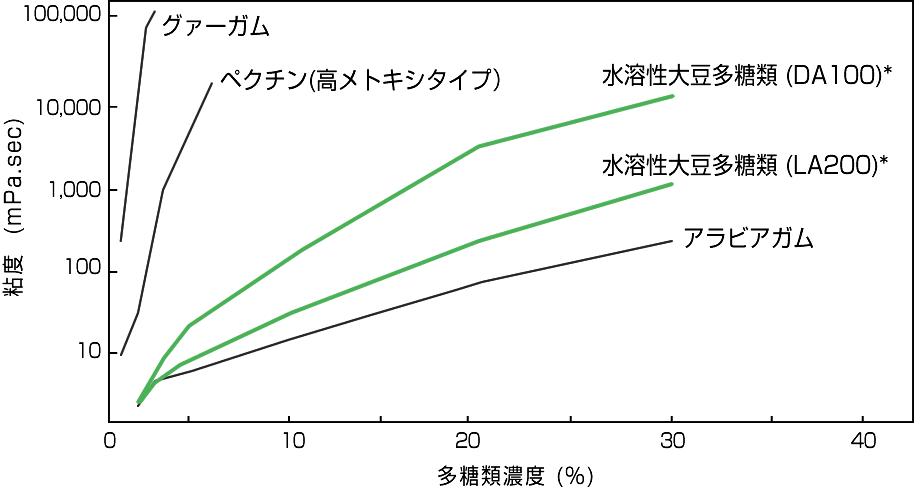
* 水溶性大豆多糖類(ソヤファイブ-Sシリーズ:不二製油 (株)にて測定)
分子構造
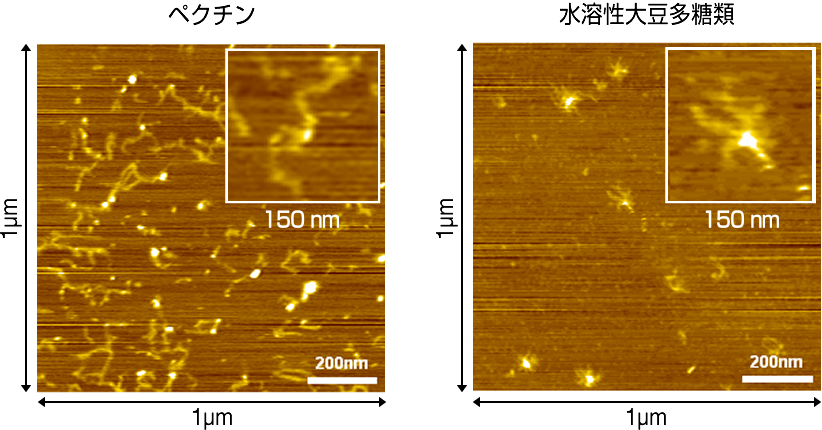
多糖類素材の特性の把握と食品における利用分野の検討において、分子のイメージを掴むことは非常に重要です。不二製油では、染色体とDNA二重ラセンの構造解析にも利用され、ナノレベルで構造を解析できる走査型プローブ顕微鏡を用いることで、水溶性大豆多糖類の分子構造を解明することに成功しています。図6に水溶性大豆多糖類、及び、ペクチンの分子の観察像を示します。水溶性大豆多糖類は、糖鎖が放射状に伸びた特徴的な星形の分子構造を持っており、直鎖の構造を持つペクチンとは大きく分子形状が異なっていることがわかります。
図6 水溶性大豆多糖類及びペクチン分子の原子間力顕微鏡
観察像
タンパク質の分散安定化とそのメカニズム
いずれの多糖類も乳酸発酵の酸性条件下では負電荷を帯びており、酸性下で正に帯電した乳タンパク質の表面に電気的に吸着し、乳タンパク質粒子の表面全体を覆うことで負に帯電させ、電荷の反発によってタンパク質の凝集を抑制していると考えられています。加えて、多糖類自身が飲料に粘度を与えることで沈殿も抑制しているのです。水溶性大豆多糖類の場合は、酸性条件下で正に帯電した乳タンパク質の表面に電気的に吸着し、タンパク質表面を覆う水溶性大豆多糖類の糖鎖(他の多糖類と違い、殆ど負電荷を帯びません)の立体障害により、タンパク質粒子どうしの会合を抑え、長期に渡って分散状態を維持すると考えられています。もともと粘度が低い水溶性大豆多糖類は、飲料に粘度を与えることが出来ないため、均質化処理を加え、乳タンパク質の粒子の大きさを沈殿しないサイズ、すなわち、1μm以下の微細粒子まで小さくすることで初めて安定性を生じます。タンパク質粒子の微細構造を観察した透過電子顕微鏡観察像を図7に示します。
図7 酸性乳飲料のタンパク質粒子の電子顕微鏡写真
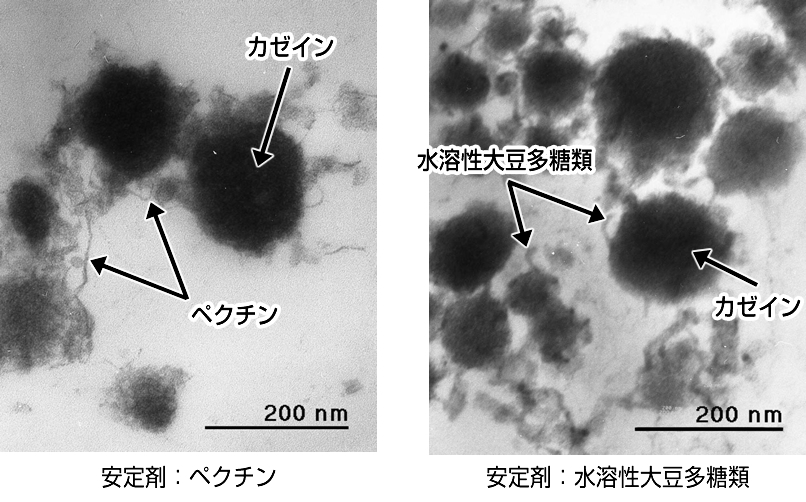
樹脂包埋切片を作成し、酢酸ウラニルで染色後に6万倍で観察した。 京都大学農学部松村教授との共同研究より






