大豆ペプチドの肉体への効果
大豆ペプチド摂取による肉体疲労軽減効果
我々が日常的に行っている歩行や走行などの全ての動作は、骨格筋の収縮によって成り立っています。そして、このような動作を継続的に実施した時のパフォーマンスの低下は「筋疲労」や「肉体疲労」と呼ばれ、極めて身近な生理現象です。その中で、遅発性筋肉痛(delayed-onset muscle soreness: DOMS)は、不慣れな運動の数日後に起こり一般的によく経験する痛みと思います(図1)。DOMSは、伸張性収縮を繰り返すことによる筋繊維上の微小な損傷が原因と考えられています 1, 2)。この損傷は骨格筋に多く含まれるクレアチンキナーゼ(CK)活性の血中における上昇を測定することにより検出できます(図2) 3)。
図1 遅発性筋肉痛
図2 遅発性筋肉痛の推測されるメカニズム
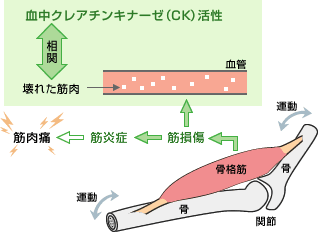
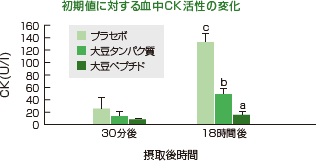
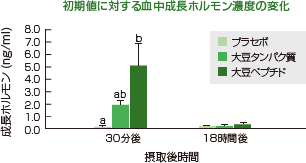
図3は、スクワット運動直後に窒素源を含まないプラセボ、大豆タンパク質、大豆ペプチドを摂取した場合の血中CK活性の運動前に対する変化量を示します 4)。プラセボ摂取群では18時間後に明確なCKの上昇が見られました。しかし、大豆タンパク質を摂取した場合、その上昇は有意に抑えられました。この結果は、大豆タンパク質の摂取により筋肉の損傷を軽減したことを示します。一方、同じ量の大豆ペプチドを摂取した場合、同じ窒素量を摂取したにもかかわらず、大豆タンパク質よりも高い効果を示しました。この結果は、大豆ペプチドの吸収性の速さに起因する効果と考えられます。一方、成長ホルモンは、筋肉細胞へのアミノ酸の輸送を増加させ、タンパク質合成を促すことが知られています。図4に示すように、大豆ペプチド摂取による効率的成長ホルモン分泌促進も、筋損傷軽減に関与していると考えられます 4)。
図3 筋肉の損傷に対する大豆ペプチドの効果
参考文献4より抜粋(一部改編)。
運動負荷:フルスクワット(25回×4), 試験飲料:運動直後に摂取, 採血:運動負荷前、30分後、18時間後, 被験者:健常男子16名, 年齢:20歳, BMI: 20.9±0.3, 運動履歴:定期的運動習慣なし
大豆タンパク質、大豆ペプチド、およびプラセボ摂取後の血中クレアチンキナーゼ活性変化。各値は初期値に対する変化量として表す。異なる文字間で有意差あり。
図4 大豆ペプチド摂取による成長ホルモン分泌促進
参考文献4より抜粋(一部改編)。
試験条件は図3と同じ。
大豆タンパク質、大豆ペプチド、およびプラセボ摂取後の成長ホルモン濃度変化。各値は初期値に対する変化量として表す。異なる文字間で有意差あり。
大豆ペプチドの筋肉疲労軽減効果については、体感効果も報告されています 5)。筋肉痛は痛覚で感じる主観的なものなので、視覚アナログスケール(visual analog scale: VAS)法によって数値化しています。VAS法とは、10 cmの線上に「0 cm」を「痛みはない」状態、「10 cm」を「これ以上の痛みはないくらい痛い(これまで経験した一番強い痛み)」状態として、現在の痛みが10 cmの直線上のどの位置にあるかを示す方法です。診療の場でも多く使われています。運動直前にプラセボもしくは大豆ペプチドを飲んでもらい、スクワット運動により誘発されるDOMSに対する効果をVAS法により検証しました。結果的に、大豆ペプチド飲料を摂取した場合、運動後1日後また2日後にプラセボ飲料に較べて筋肉痛が減少しました(図5)。なお、図6はスクワット運動後の血中アミノ酸濃度の変化を分析した結果です。大部分のアミノ酸で運動前に対し減少しました。しかし、10%以上の顕著な減少が見られたアミノ酸は、含流アミノ酸であるメチオニンと分岐鎖アミノ酸、トリプトファンを除いた芳香族アミノ酸でした。これらは大豆ペプチド摂取で特に速やかに吸収されるアミノ酸種です。運動により特に消費されるアミノ酸の速やかな補給が、大豆ペプチド摂取による筋肉痛軽減効果の一因と考えられます。
図5 大豆ペプチド摂取による遅発性筋肉痛軽減効果
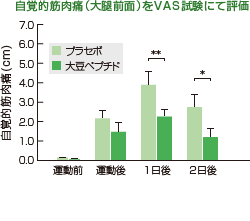
参考文献5より抜粋。
運動負荷:フルスクワット(20回×7、インターバル2min),試験飲料:運動直前に摂取
採血:運動負荷前、運動直後、1日後、2日後, ウォッシュアウト期間:1ヶ月
被験者:健常女子16名, 年齢:22.2 ± 0.8, BMI: 19.8±0.7, 運動履歴:定期的運動習慣なし
運動前、運動直後、1日後、および2日後の大腿前面の自覚的筋肉痛をVAS法で評価。
群間の有意差(*P < 0.1、**P < 0.05)。
図6 運動後の血中アミノ酸濃度変化
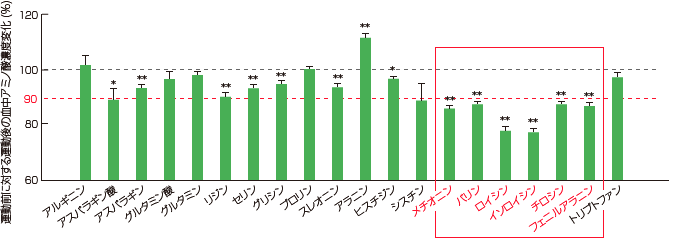
参考文献5より抜粋。試験条件は図5と同じ。
運動前(試験飲料摂取前)に対する運動後の血中アミノ酸の変化率を示す。
群間の有意差(*P < 0.05、**P < 0.01)。
運動と大豆ペプチドの組み合わせによるサルコペニア予防の可能性
日本の65歳以上の高齢者数は2012年時点で3,000万人を超え、全人口に占める高齢率は24.1%です。今後も高齢化は加速的に進み、2060年には高齢化率は39.9%に達し、2.5人に1人が65歳以上となると予想されています。ロコモティブシンドロームとは「運動器の障害により要介護になるリスクの高い状態になること」を指し、2007年に日本整形外科学会が新たに提唱した概念です。ロコモティブシンドロームの主要因として骨粗鬆症、関節トラブル、そして加齢にともなう骨格筋の減少(サルコペニア)が挙げられます。これらの要因は個別に独立しているのではなく、筋肉の減少で関節の負担が増し、関節が痛むので活動量が低下して筋肉が減少するといったように密接に関連しています。よって、何らかの対策を講じないと負のスパイラルが止められずに寝たきりのリスクが増大していく一方になります。
サルコペニアの成因は複雑ですが、身体的不活発とタンパク・エネルギー低栄養の2つが重要な要因と考えられています。上記要因によりサルコペニアを合併しやすい虚弱高齢者に対し、筋力向上トレーニングプログラムに大豆ペプチドの栄養介入を加え、その相加効果を検討した研究をご紹介します 6)。年齢が70歳以上で過去1年以内に1回以上の転倒経験者を運動プログラムのみの群と運動+週4本の大豆ペプチド飲料(大豆ペプチドとして1回8g摂取)を摂取した群に分け、介入前後で各種パラメーターを測定しました。その結果、表1に示すように、12週間の介入プログラム実施前後で通常歩行速度、膝伸展力、および白血球総数において、運動群および運動+大豆ペプチド群とも改善する傾向が見られましたが、運動+大豆ペプチド群における変化のみ統計学的有意差が確認されました。さらに、両群の変化量(介入後-介入前)を比較したところ、いずれの変化量も運動+大豆ペプチド群の方が大きく、特に白血球数の変化量の群間差は有意差が確認されました(図7)。総白血球数は、体内の炎症性負荷を反映するマーカーです。運動+大豆ペプチド群において総白血球数が有意に減少したことは、運動トレーニングに大豆ペプチドを併用することで、体内の炎症反応が抑制されたことを示唆します。なお、上記の結果との関連は不明ですが、大豆ペプチド由来のトリペプチドVal-Pro-Tyrが、炎症性サイトカインの分泌抑制効果を有することが報告されています 7)。以上の結果から、運動トレーニング直後に大豆ペプチドを摂取することで、運動トレーニング効果(下肢機能の向上、体内炎症反応の抑制)が増強される可能性が示されました。
図7 運動と運動+大豆ペプチド群における3指標の変化量(介入後-介入前)の比較
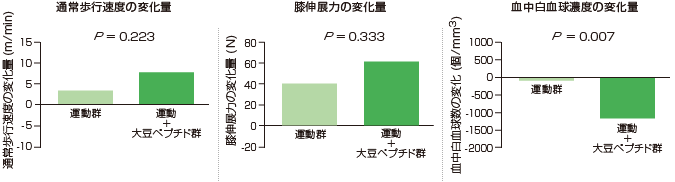
参考文献6より抜粋。
表1 転倒経験者群内における運動群 vs. 運動+大豆ペプチド群
| 調査項目 | プログラム | 介入前調査 | 介入後調査 | 前値 vs 後値 (P値) |
|---|---|---|---|---|
| 通常歩行速度 (m/秒) |
運動 運動+大豆ペプチド |
71.1 ± 14.1 70.9 ± 12.5 |
74.3 ± 13.9 78.5 ± 18.9 |
0.136 0.035 |
| 膝伸展力 (N) |
運動 運動+大豆ペプチド |
205 ± 111 178 ± 041 |
245 ± 89 237 ± 52 |
0.091 0.002 |
| 白血球総数 (/mm3) |
運動 運動+大豆ペプチド |
6040 ± 1080 6570 ± 0910 |
5970 ± 1280 5410 ± 1110 |
0.712 0.001 |
値は平均値±標準偏差。介入前データはすべて群間差無し(Wilcoxonの順位和検定)。
前値 vs. 後値(P値)は各群内の前後の値をWilcoxonの符合付き順位和検定で導いた有意水準。
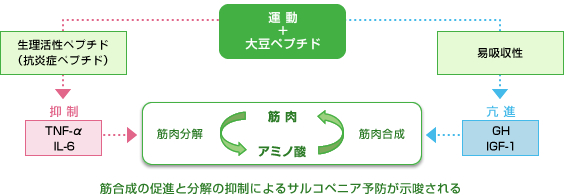
サルコペニアは加齢に伴い、筋タンパク合成因子(運動、IGF-1、テストステロン、ビタミンD、アミノ酸など)が減少する一方で、各種疾病の増加により炎症性サイトカイン(TNF-α、IL-6など)が増加し、筋タンパク分解が合成を上回ることで発症すると考えられています。先に記載したように、大豆ペプチドはアミノ酸の供給源として、また成長ホルモンを介したIGF-1分泌促進により、筋タンパク合成を促すと考えられます。一方、大豆ペプチド由来生理活性ペプチドにより炎症性サイトカインの分泌を抑制することで、筋タンパクの分解を抑制することが示唆されます(図8)。
図8 大豆ペプチドと運動の組み合わせによるサルコペニア予防の可能性
参考文献
Armstrong R.B.: Mechanisms of exercise-induced delayed onset muscular soreness: a brief review, Med. Sci. Sports Exerc., 16, 529–38 (1984).
MacIntyre D.L., Reid W.D., McKenzie D.C.: Delayed muscle soreness. The inflammatory response to muscle injury and its clinical implications, Sports Med., 20, 24–40 (1995).
Clarkson P.M., Nosaka K., Braun B.: Muscle function after exercise-induced muscle damage and rapid adaptation, Med. Sci. Sports Exerc., 24, 512–20 (1992).
Masuda K., Maebuchi M., Samoto M., Ushijima Y., Uchida Y., Kohno M., Ito R., Hirotsuka M.: Effect of soy-peptide intake on exercise-induced muscle damage. Jpn. J. Clin. Sports Med., 15, 228-235 (2007).
Nakanishi Y, Shirakawa S, Maebuchi M, Okubo M, Ikeda T, Inage H, Suzuki M., Samoto M., Kimura S.: Effects of soy protein intake in peptide form on delayed-onset muscle soreness induced by eccentric exercise. J. Sport Sci. Osteo. Thera., 13, 9-19 (2011).
Shinkai S., Kim H., Watanabe N., Lee S., Saito K., Suzuki T.: Randomized controlled trial on the effects of resistance training with or without nutritional supplementation of soy peptide for the frail elderly. Jpn. J. Nutr. Diet., 67, 76-83 (2009).
Kovacs-Nolan J., Zhang H., Ibuki M., Nakamori T., Yoshiura K., Turner P. V., Matsui T., Mine Y.: The PepT1-transportable soy tripeptide VPY reduces intestinal inflammation. Biochim. Biophys. Acta., 1820, 1753-1763 (2012).





